ホーム > トピック・関連情報 > プレスリリース > 患者から分離された新型コロナウイルス・オミクロン/BA.2変異株の性状解明
患者から分離された新型コロナウイルス・オミクロン/BA.2変異株の性状解明
~オミクロン/BA.1変異株と同程度の病原性であることが明らかに~
2022年5月17日
東京大学医科学研究所
国立国際医療研究センター
国立感染症研究所
1. 発表者:
河岡 義裕(東京大学医科学研究所 ウイルス感染部門 特任教授
国立国際医療研究センター 国際ウイルス感染症研究センター長)
鈴木 忠樹(国立感染症研究所 感染病理部 部長)
2. 発表のポイント :
- 現在流行しているBA.2系統に属するオミクロン株(オミクロン/BA.2株)(注1)を患者から分離し、その性状を解析した。オミクロン/BA.2株を感染させた動物では、体重減少と呼吸器症状の悪化がみられないなど、その病原性は従来株よりも低く、12月から2月にかけて流行していたBA.1系統のオミクロン株(オミクロン/BA.1株)と同程度であることが明らかとなった。
- 抗体薬(注2)のカシリビマブ・イムデビマブ、チキサゲビマブ・シルガビマブ、ソトロビマブは、オミクロン/BA.2株を感染させたハムスターの肺における増殖を抑制した。
- 抗ウイルス薬(注3)のモルヌピラビル (メルク)、ニルマトレルビル (ファイザー)、S-217622 (塩野義)は、オミクロン/BA.2株を感染させたハムスターの肺における増殖を抑制した。
3.発表概要
東京大学医科学研究所ウイルス感染部門の河岡義裕特任教授らの研究グループは、新型コロナウイルス変異株・オミクロン株/BA.2の特性を明らかにしました。
2021年末に新型コロナウイルスの変異株・オミクロン株が南アフリカで確認されて以降、現在(2022年5月時点)も本変異株による爆発的流行が世界規模で続いています。オミクロン株は、少なくとも6つの系統(BA.1、BA.1.1、BA.2、BA.3、BA.4、BA.5)に分類されます。オミクロン株の流行が始まってから数ヶ月間は、BA.1系統に属する株(オミクロン/BA.1株)が世界の主流でしたが、1月上旬からBA.2系統に属する株(オミクロン/BA.2株)の感染例が増加し始め、2022年5月現在はオミクロン/BA.2株が世界でもっとも流行しています。
本研究グループは今回、流行しているオミクロン/BA.2株を患者から分離し、その性状を新型コロナウイル感染症(COVID-19)の動物モデル(マウスおよびハムスター)を用いて評価し、パンデミック初期の流行株(従来株)およびオミクロン/BA.1株と比較しました。
その結果、オミクロン/BA.2株は、マウスやハムスターの上気道および下気道部で増殖するものの、その増殖力と病原性は、従来株よりも低く、オミクロン/BA.1株と同程度であることが明らかになりました。また、抗体薬のカシリビマブ・イムデビマブ、チキサゲビマブ・シルガビマブ、ソトロビマブや、抗ウイルス薬のモルヌピラビル (メルク)、ニルマトレルビル (ファイザー)、S-217622 (塩野義)は、オミクロン/BA.2株を感染させたハムスターの肺における増殖を抑えることを明らかにしました。
本研究成果は、オミクロン株BA.2系統のリスク評価など行政機関が今後の新型コロナウイルス感染症対策計画を策定、実施する上で、重要な情報となるだけでなく、医療現場における適切なCOVID-19治療薬の選択に役立つと期待されます。本研究成果は、2022年5月16日、英国科学雑誌「Nature」オンライン速報版で公開されました。
なお、本研究は、東京大学、国立感染症研究所、国立国際医療研究センター、米国ウィスコンシン大学、米国ワシントン大学、米国ユタ州立大学、米国ミシガン大学、米国国立衛生研究所、永寿総合病院が共同で行ったものです。また、本研究は、日本医療研究開発機構(AMED)新興・再興感染症に対する革新的医薬品等開発推進研究事業並びに厚生労働科学研究費補助金新興・再興感染症及び予防接種政策推進研究事業の一環として行われました。
4.発表内容:
2021年11月に、新型コロナウイルスのスパイク蛋白質(注4)に少なくとも30ヶ所の変異を有するオミクロン株が南アフリカで初めて確認されました。オミクロン株は、少なくとも6つの系統(BA.1、BA.1.1、BA.2、BA.3、BA.4、BA.5)に分類されます。オミクロン株の流行が始まってから数ヶ月間は、BA.1系統に属する株(オミクロン/BA.1株)が主流でしたが、1月上旬からBA.2系統に属する株(オミクロン/BA.2株)の感染例が増加し始め、2022年5月現在オミクロン/BA.2株が世界でもっとも流行しています。
ウイルス感染にとって重要な役割を担うスパイク蛋白質上の変異は、病原性や伝播力を変化させる可能性や既存のワクチンや治療薬の効果を減弱させる可能性がありますが、オミクロン/BA.2株の基本性状は明らかにされていませんでした。そこで、東京大学医科学研究所ウイルス感染部門の河岡義裕特任教授らの研究グループは、COVID-19感染モデル動物のマウスとハムスターを用いて、現在流行しているオミクロン/BA.2株を患者から分離し、その増殖能と病原性を従来株やオミクロン/BA.1株と比較しました。マウスの肺や鼻におけるオミクロン/BA.2株の増殖能は、オミクロン/BA.1株と同程度もしくはやや低いことが明らかとなりました(図1)。また、オミクロン/BA.2株を感染させたマウスでは、呼吸器症状の悪化も認められませんでした(図1)。
続いてハムスターを用いて同様の解析を行い、オミクロン/BA.1株と比較しました。患者から分離されたオミクロン/BA.2の4株をハムスターに感染させたところ、オミクロン/BA.1株と同様に、全ての株において感染ハムスターは体重減少を示しませんでした (図2)。また、オミクロン/BA.2株の、ハムスター呼吸器での増殖能はオミクロン/BA.1株よりもやや低いことがわかりました(図2)。さらにコンピュータ断層撮影法(CT)を用いて、感染動物の肺を解析したところ、オミクロン/BA.2株感染ハムスターでは、オミクロン/BA.1株感染ハムスターと同程度の軽度の炎症しか見られませんでした。ヒトのhACE2を持つハムスターを用いた感染実験においても、オミクロン/BA.2株の病原性と増殖能は従来株よりも低く、オミクロン/BA.1株と同程度であることが明らかとなりました。
次に、mRNAワクチンを接種したヒトや新型コロナウイルスに感染したヒトの血清・血漿中の抗体の、様々な新型コロナウイルス株に対する中和活性(注 5)を解析しました。その結果、これらの血清・血漿の、オミクロン株3系統(BA.1、BA.1.1、BA.2)に対する中和活性は、従来株やデルタ株(注 6)に対する活性よりも低いことが明らかになりました(図3)。
最後に、抗体薬や抗ウイルス薬がオミクロン/BA.2株に有効であるか、ハムスターモデルを用いて検証しました。現在国内では、カシリビマブ・イムデビマブ、ソトロビマブの抗体薬、あるいはレムデシビル、モルヌピラビル、ニルマトレルビル・リトナビルの抗ウイルス薬が COVID-19 に対する治療薬として承認を受けています。しかし、これらの治療薬がオミクロン/BA.2株に対して有効かどうかについては、動物レベルでは明らかにされていませんでした。抗体薬のカシリビマブ・イムデビマブ、チキサゲビマブ・シルガビマブ、あるいはソトロビマブを、オミクロン/BA.2株を感染させたハムスターに投与したところ、いずれもハムスターの肺におけるウイルス増殖を抑えることが明らかとなりました。一方で、鼻での増殖を抑えることはできませんでした。続いて抗ウイルス薬3種類(モルヌピラビル、ニルマトレルビル、臨床試験中のS-217622)の効果を検証したところ、全ての薬剤でハムスターの肺におけるウイルス増殖が大幅に抑制されました。また、ニルマトレルビルとS-217622は、鼻での増殖も抑制することがわかりました(図4)。
本研究グループは、患者から分離した複数のオミクロン/BA.2株の増殖能と病原性について、複数のCOVID-19動物モデルを用いて解析し、オミクロン/BA.1株と同程度であることを明らかにしました。また、動物モデルを用いて、抗体薬と抗ウイルス薬がオミクロン/BA.2株に対して治療効果を有することを明らかにしました。
スパイクタンパク質のみを従来株と置き換えた組換えウイルスを用いた実験で、オミクロン/BA.2株のスパイクタンパク質を有するウイルスの病原性がオミクロン/BA.1株のスパイクタンパク質を有するウイルスよりも病原性が高いとする報告もありますが、患者から分離されたウイルスを用いた本研究ではオミクロン/BA.2株とオミクロン/BA.1株は同程度の病原性であることが明らかになりました。本研究では、組換えウイルスではなく、患者から分離されたオミクロン/BA.2ウイルスそのものを用いた解析を行っているため、より実際の臨床現場における病態を反映していると考えられます。
現在、オミクロン/BA.2株とオミクロン/BA.1株の組換え体であるXE株など新たな変異株の感染が国内で確認されています。今後の流行が懸念される変異株について、どのような性状を示すのか引き続き検証していく必要があります。本研究を通して得られた成果は、変異株のリスク評価など行政機関が今後のCOVID-19対策計画を策定、実施する上で、重要な情報となります。
5.発表雑誌:
- 雑誌名:「Nature 」 5月16日オンライン速報版
- 論文タイトル:Characterization and antiviral susceptibility of SARS-CoV-2 Omicron/BA.2
- 著者:
Ryuta Uraki*, Maki Kiso*, Shun Iida*, Masaki Imai*, Emi Takashita*, Makoto Kuroda*, Peter J. Halfmann, Samantha Loeber, Tadashi Maemura, Seiya Yamayoshi, Seiichiro Fujisaki, Zhongde Wang, Mutsumi Ito, Michiko Ujie, Kiyoko Iwatsuki-Horimoto, Yuri Furusawa, Ryan Wright, Zhenlu Chong, Seiya Ozono, Atsuhiro Yasuhara, Hiroshi Ueki, Yuko Sakai-Tagawa, Rong Li, Yanan Liu, Deanna Larson, Michiko Koga, Takeya Tsutsumi, Eisuke Adachi, Makoto Saito, Shinya Yamamoto, Masao Hagihara, Keiko Mitamura, Tetsuro Sato, Masayuki Hojo, Shin-ichiro Hattori, Kenji Maeda, Riccardo Valdez, IASO study team, Moe Okuda, Jurika Murakami, Calvin Duong, Sucheta Godbole, Daniel C. Douek, Ken Maeda, Shinji Watanabe, Aubree Gordon, Norio Ohmagari, Hiroshi Yotsuyanagi, Michael S. Diamond, Hideki Hasegawa, Hiroaki Mitsuya, Tadaki Suzuki, and Yoshihiro Kawaoka¶
*:筆頭著者
¶:責任著者 - DOI: 10.1038/s41586-022-04856-1
- URL: https://www.nature.com/articles/s41586-022-04856-1
6.お問い合わせ先
- 研究に関するお問い合わせ
東京大学医科学研究所 ウイルス感染部門
特任教授 河岡 義裕(かわおか よしひろ)
E-mail::kawaoka@ims.u-tokyo.ac.jp
※なるべくメールでお問い合わせください。 - 報道に関するお問い合わせ
東京大学医科学研究所 国際学術連携室(広報)
清水麻子
Tel:090-9832-9760
E-mail:koho@ims.u-tokyo.ac.jp - 国立国際医療研究センター
企画戦略局広報企画室:西澤樹生
Tel:03-3202-7181 <平日9時0分~17時0分>
E-mail:press@hosp.ncgm.go.jp
7.用語解説:
(注1)BA.2系統に属するオミクロン株(オミクロン/BA.2株):
ウイルス感染は、コロナウイルス粒子表面に存在するスパイク蛋白質を介してウイルス粒子が宿主細胞表面の受容体蛋白質に結合することで始まる。実用化されたあるいは開発中のCOVID-19 に対する抗体薬は、このスパイク蛋白質を標的としており、その機能を失わせる(中和する)ことを目的としている。オミクロン/BA.2株のスパイク蛋白質は、パンデミック初期の株と比較すると、少なくとも 31 ヶ所の変異を有している。一方、オミクロン/BA.1株と比較すると、11ヶ所の違いがある。
(注2)抗体薬:
カシリビマブ・イムデビマブ(販売名:ロナプリーブ注射液セット)は令和3年7月19日に特例承認を受けた。ソトロビマブ(販売名:ゼビュディ点滴静注液)は令和3年9月27日に特例承認を受けた。チキサゲビマブ・シルガビマブ(開発コード:AZD7442)は臨床試験中。 https://www.mhlw.go.jp/content/10900000/000938454.pdfを参照。
(注3)抗ウイルス薬:
レムデシビル(販売名:ベクルリー点滴静注液)は令和2年5月7日に特例承認を受けた。モルヌピラビル(販売名:ラゲブリオ)は令和3年12月24日に特例承認を受けた。ニルマトレルビル・リトナビル(販売名:パキロビッドパック)は令和4年2月10日に特例承認を受けた。S-217622は臨床試験中。https://www.mhlw.go.jp/content/10900000/000938454.pdfを参照。
(注4)スパイク蛋白質:
コロナウイルス粒子表面に存在する蛋白質。ウイルスが宿主細胞に侵入・感染する際に要となる蛋白質であり、スパイク蛋白質上のアミノ酸変異は病原性や伝播性に影響を与えることが報告されている。
(注5)中和活性:
抗体が持つウイルスの細胞への感染を阻害する機能。
(注6)デルタ株:
2020年12月にインドで最初に検出されたB.1.617.2系統に分類されるデルタ株は、オミクロン株が出現するまで世界で最も流行していた変異ウイルスである。デルタ株に存在するスパイク蛋白質の特定の変異(L452RやP681R)がデルタ株の増殖性や伝播効率の上昇に寄与する可能性が示唆されている。
8.添付資料:
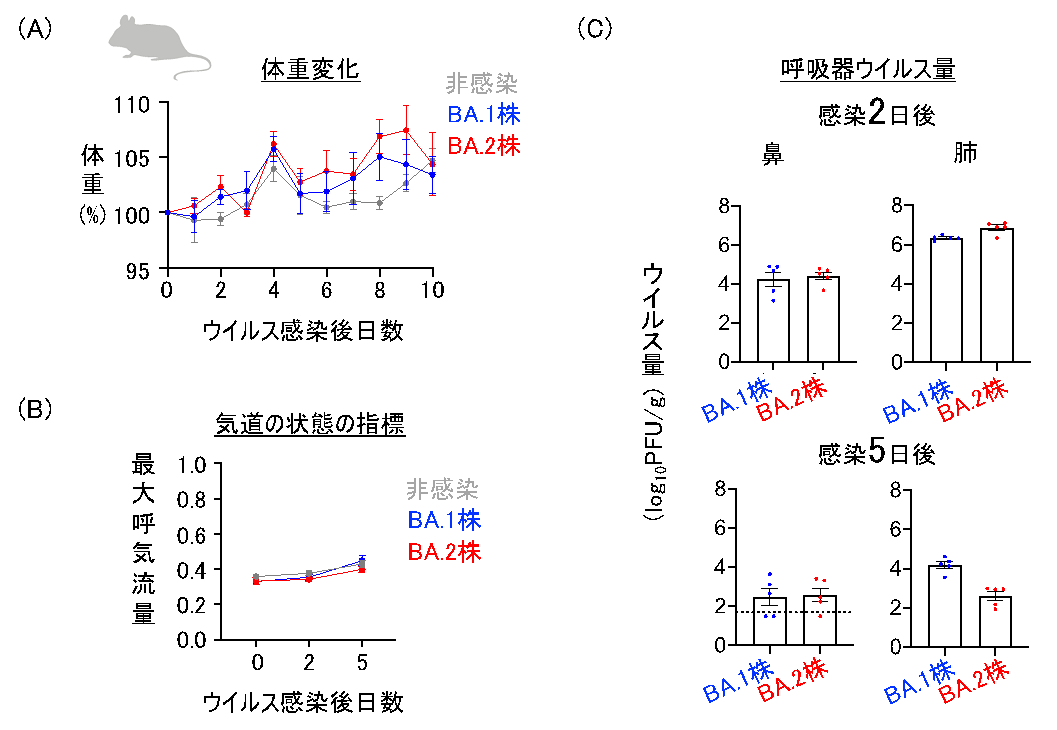
図1 野生型マウスにおけるオミクロン/BA.2株の病原性と増殖力
新型コロナウイルス・オミクロン/BA.2株をマウスの鼻腔内に接種した。(A)接種後、非感染動物(対照群)と感染動物の体重を毎日測定した。オミクロン/BA.2感群ではオミクロン/BA.1感染群と同様に体重減少は認められなかった。(B)呼吸機能の評価指標の1つである最大呼気流量は、気道の状態を測定できる指標である。オミクロン/BA.2株では感染後の低下は認められず、非感染マウスやオミクロン/BA.1株感染マウスと同程度であった。(C)感染後2日目または5日目の鼻と肺におけるウイルス量を測定した。 オミクロン/BA.2株はオミクロン/BA.1株と同程度の増殖能を示した。
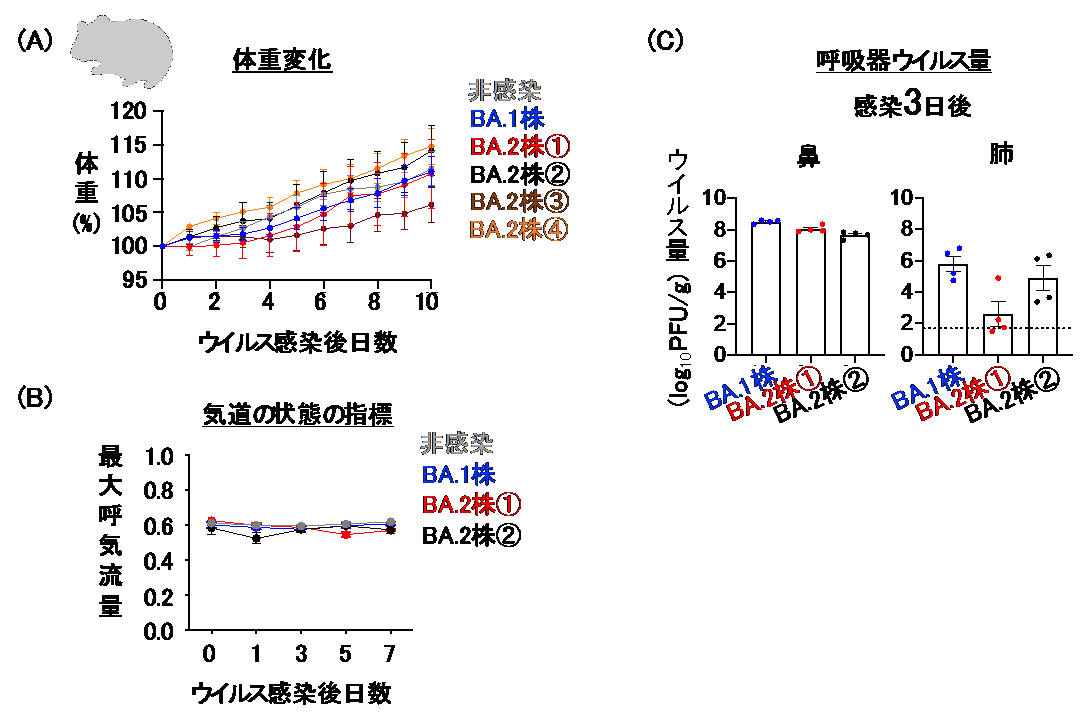
図2 野生型ハムスターにおけるウイルスの病原性と増殖力
新型コロナウイルス・オミクロン株をハムスターの鼻腔内に接種した。(A)接種後、非感染動物(対照群)と感染動物の体重を毎日測定した。オミクロン/BA.2感染群ではオミクロン/BA.1感染群と同様に全ての株で体重が増加した。(B)呼吸機能の評価指標の1つである最大呼気流量は、気道の状態を測定できる指標である。オミクロン/BA.2株の2株ともに感染後の低下は認められず、非感染動物やオミクロン/BA.1株感染動物と同程度であった。(C)感染後3日目の鼻と肺におけるウイルス量を測定した。オミクロン/BA.2株の増殖能はオミクロン/BA.1株と同程度かやや低かった。
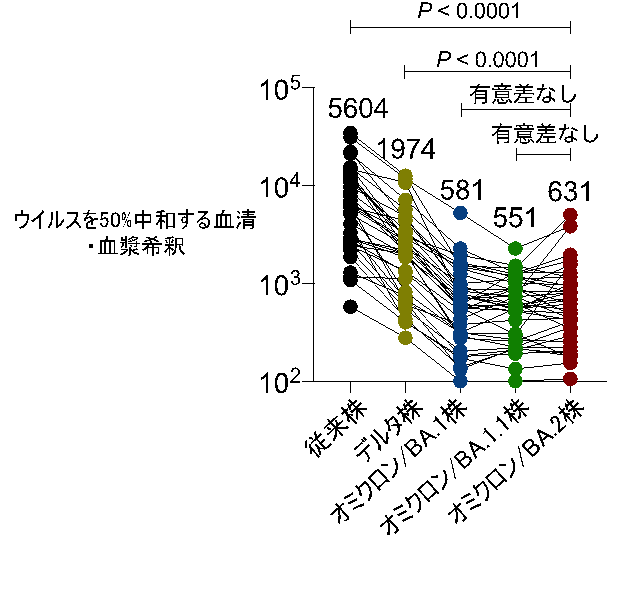
図3 mRNAワクチンを3回接種したヒトで誘導された抗体のオミクロン/BA.2株に対する中和活性
mRNAワクチンを3回接種したヒトの血清や血漿と、新型コロナウイルスを混合し、ウイルスを50%中和する血清・血漿希釈を算出した。オミクロン/BA.2株に対する中和活性は、従来株やデルタ株に対する中和活性よりも低く、オミクロン/BA.1株やオミクロン/BA1.1株に対する中和活性と同程度だった。
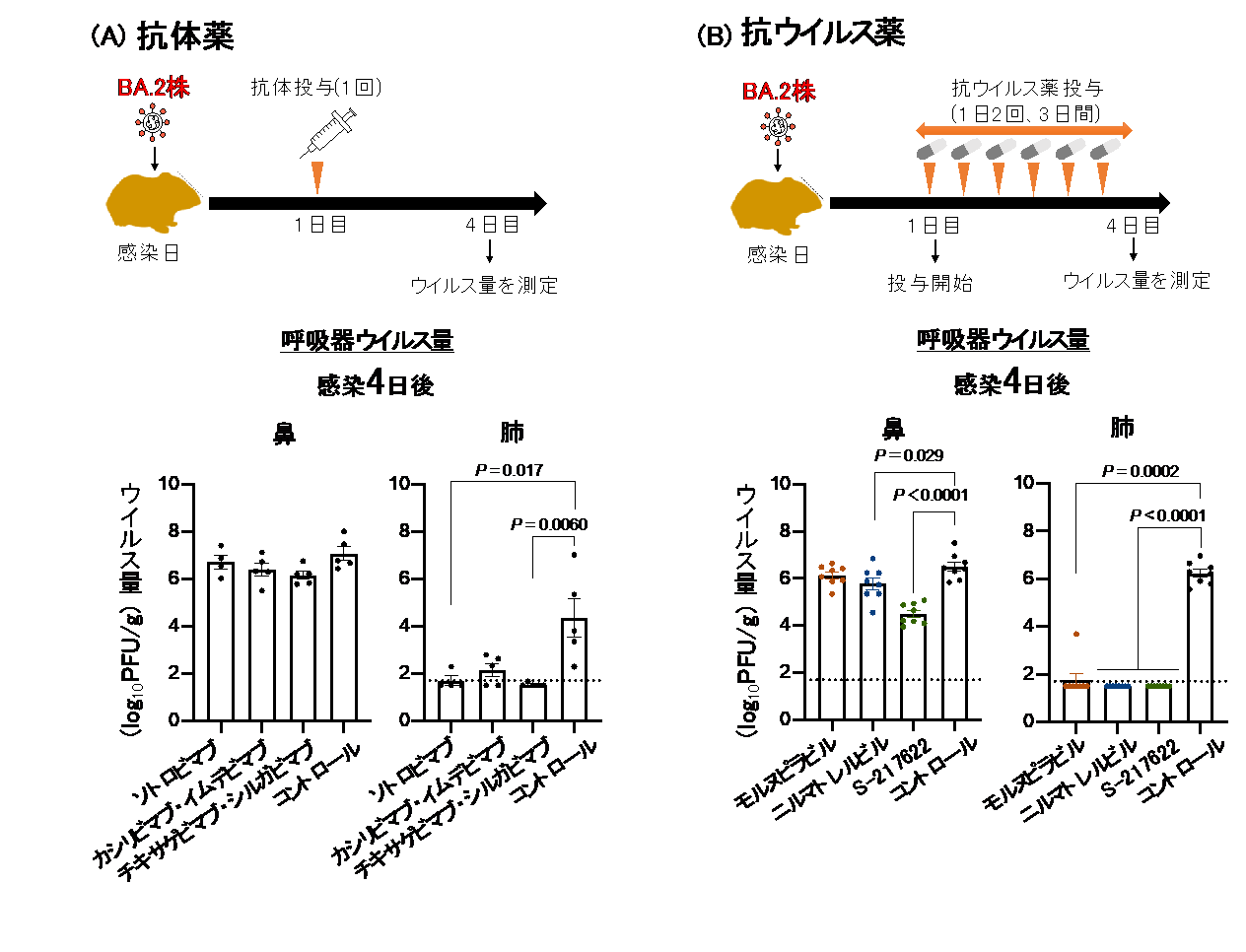
図4 野生型ハムスターにおける抗体薬や抗ウイルス薬の効果の検証
新型コロナウイルス・オミクロン/BA.2株をハムスターの鼻腔内に接種し、接種1日後に抗体薬(1回)もしくは抗ウイルス薬(3日間)を投与した。(A) ウイルス接種4日目の鼻と肺におけるウイルス量を測定した。カシリビマブ・イムデビマブ、チキサゲビマブ・シルガビマブ、ソトロビマブは、ハムスターの肺におけるウイルス増殖を抑えた。一方で、鼻での増殖を抑えなかった。 (B) ウイルス接種4日目の鼻と肺におけるウイルス量を測定した。 モルヌピラビル、ニルマトレルビル、臨床試験中のS-21762は、いずれもハムスターの肺におけるウイルス増殖を大幅に抑制した。また、ニルマトレルビルとS-217622は、鼻での増殖も抑制した。














